Нийгмийн Эрүүл Мэндийн Хүрээлэн, "Гялс" Анагаах ухааны төв, ХХК
It is the second part of a comprehensive levlew of literature on the utilization of cancer serum markets, including CA-19-9, CA-125, CA-15-3, human chorionic gonadotropine, placental alkaline phosphotase and neurone-specific enolase for clinical and public health purposes. Unpublished results of the authors on the first in Mongolia qualitative determinations of CA-19-9, CA-125, CA-15-3, human chorionic gonadotropine in sera of patients with different clinical diagnosis have been disscussed in comparison with the literature data.
Pp. 19-22, . Tables:5-6, Literature: 44-84;
Тодорхойлолт
Хүний бүдүүн гэдэсний аденокарциномын эдээс гаралтай SW1116 эсийн есгөврөөр дархлаажуулсан хулганын дэлүүний эсээс АНУ-ын нэрт биологич, вирус судлалч Х.Копровскийн Лабораторид ялгасан 2000 гаруй моноклон эсрэгбиеийн NS 19-9 хэмээн тэмдэглэсэн нэг клон иь бүдүүн гэдэсний хорт хавдрын эсийг сонгон таних чадвартайг анх 1979 онд илрүүлэн бичжээ (44). Цаашдын судалгаагаар энэ эсрэгтөрөгч нь хоол боловсруулах замын хучуур эсийн сарьсны бүтцэнд ордог гликопротейн (муцин) бөгөөд эсрэгтөрөгчийн детерминант нь цусны Льюс (Lewis) бүлгийн эсрэгтөрөгчтэй төстэй бүтэцтэй сиалжсан пентасахарид гликозид болохыг тогтоосон юм (45, 46, 47). Энэ ИХМ-ыг анх илрүүлсэн Копровскийн лабораторийн судлаачид GIGA (gastro intestinal cancer-associated antigen - ходоод-гэдэсний хавдарын эсрэгтөрөгч) гэж нэрлэх хандлагатай байсан (48, 49) боловч худалдаанд гарсан анхны РИА оношлуур үйлдвэрлэсэн CENTOCOR компани оношлуураа СА (cancer or carbohydrate antigen - өмөнгийн буюу нүүрс-уст эсрэгтөрөгч) 19-9 хэмээн нэрийдсэнээр энэ нэр томъёог нийтээр хэрэглэх болжээ.
Эмнэлзүйн холбогдол. СА19-9 эрүүл хүмүүсийн 99,6%-ынх нь цусны ийлдсэнд 37 IU/ml хүртэл хэмжээгээр тодорхойлогдож болно (2, 3). Гэхдээ энэ хэмжээ нь цусны Льюс бүлгийн генотип, секретор статусаас хамаарах бөгөөд кавказоид хүн амын дотор 7% орчим тохиолддог Le(a-b-) генотиптэй үед ийлдэс болон шүлс зэрэг биеийн бусад шингэнд СА 19-9 тодорхойлогддоггүй (50, 51) бол хэвийн үедэх СА 19-9~ийн ийлдсэндэх хэмжээ нь Le(a-b+) генотиптэй буюу секретор хүмүүст Le(a+b-) генотиптэй буюу секретор биш хүмүүсийнхээс 5 дахин бага (дээд хязгаар нь 12,4 болон 61,2 IU/ml) байдаг байна (52).
Ийлдсэндэх СА 19-9-ийн хэмжээ нь хоол боловсруулах замын хорт хавдруудын үед, тухайлбал нойр булчирхайн өмөнгийн 73-79%-д, цөсний замын өмөнгийн 73%-д, ходоодны өмөнгийн 42-65%-д, бүдүүн гэдэсний өмөнгийн 18-37%-д, элэгний өмөнгийн 22%-д тус тус хэвийнхээс ихэсдэг бөгөөд ийлдсэндэх хэмжээ нь хавдрын хэмжээ, үсэрхийлэлийн тархалттай шууд хамааралтай байдаг ажээ (2). Тиймээс энэ ИХМ-ыг нойр булчирхайн өмөн(НБӨ)-ийн оношийг баталгаажуулах, эмчилгээний үр дүнг хянах зорилгоор голдуу хэрэглэдэг.
Давсагны хорт хавдрын үед шээсэндэх СА 19-9-ийн хэмжээ мөн ихэсдэг байна (53, 54, 55).
Тарвалзүйн холбогдол СА19-9 нь эрхтэн өвөрмөц чанар багатай тул тарвалзүйн тандалтанд өргөн ашигладаггүй (2).
Манайд судлагдсан байдал. Манай улсад СА19-9-ийг судласан материалыг бид хэвлэлээс олсонгуй.
“Гялс" Анагаах ухааны төв, ХХК-д 1998 оны 12 дугаар сараас СА-19-9-ийг Францийн bioMerieux компанийн mini-VIDAS хэмээх ФХТЭБУ-ын бүрэн автоматаар тодорхойлж байна.1999 оны 8 дугаар cap хүртлэх хугацаанд хоол боловсруулах замын эмгэгийн онош тодруулах заалттай нийт 20 сорьцонд шинжилгээ хийхэд хэвийн хэмжээний дээд хязгаар(37 lU/ml)-aac давсан тохиолдол гараагүй бөгөөд дунджаар 6,0 IU/ml тодорхойлогдсон байна. Шинжлүүлэгсэдийн дотор НБӨ оноштой өвчтөн байгаагүй болно. НБӨ-ийн эмнэлзүйн оношлогоо амаргүйг харгалзан үзвэл, энэ ИХМ-ыг манай нөхцөлд хоол боловсруулах замын, нэн ялангуяа нойр булчирхайн төрөл бүрийн эмгэгийн үед судлаж, оношзүйн шалгуур боловсруулан эмнэлзүйн практик нэвтрүүлэх шаардлага тулгарч байна.
Toдохойлолт. Энэ эсрэгтөрөгч нь өндөр молекул жинтэй (250-300 kDA) гликопротейн (муцин) бөгөөд өндгөвчийн цисто-аденокарциномын эдээс гаралтай OVCA 433 эсийн өсгөврөөр дархлаажуулсан BALB/c хулганын дэлүүний эсээс гарган авсан ОС 125 моноклон эсрэгбиеэр анх илрүүлжээ (56). СА 125 гэдэг нэрийг мөн CENTOCOR компани өгсөн байна.
Эмнэлзүйн холбогдол СА 125 нь хүний үр хөврөлийн козломик эдийн хэвийн бүтээгдэхүүн бөгөөд насанд хүрсэн эрүүл хүмүүст 35 IU/ml хүртэл хэмжээгээр илэрч болдог (2, 3, 57). Ингэхдээ төрөх насны эмэгтэйчүүдэд ялигүй их (дунджаар 38 IU/ml), цэвэршсэнээс хойших. насны эмэгтэйчүүдэд арай бага (дунджаар 31 IU/ml), эрэгтэйчүүдэд бүр бага (дунджаар 28 IU/ml) тодорхойлогддог байна (58).
Энэ эсрэгтөрөгчийг өндгөвчийн өмөн (ӨӨ)-гийн өвөрмөц маркер гэж үзэж, ӨӨ-ийн оношлогоо, явцын хяналт, эмчилгээний үр дүнг хянахад өргөн хэрэглэдэг боловч биений юм ирэх үе, өндгөвчийн үрэвсэлт өвчин, хоргүй хавдруудын үед мөн ихэсч болдгийг судлаачид тэмдэглэсэн байна (2, 3, 150 57). Тиймээс Хавдрын маркерийн Хамбургийн бүлгийн зөвшилцлийн зөвлөмжөөр СА 125-ын ийлдсэндэх хэмжээ >150 IU/ml байх нь ӨӨ байх 95% магадлалтай гэж тогтжээ (59).
Тарвалзүйн холбогдол ӨӨ илрүүлэх тандалтанд СА 125-ыг амжилттай хэрэглэж эхлэж байна. Их Британид 45-аас дээш насны 22 000 эмэгтэй
хамруулан дунджаар 7 жил хийсэн нэг тандалт судалгаагаар анхны шинжилгээгээр ийлдсэндэх СА 125-ын хэмжээ >30 IU/ml юм уу, >100 IU/ml байх нь нэг жилийн дотор ӨӨ-өөр өвчлөх эгзэгийг 35,9 болон 204,8 дахин ихэсгэж байгаа дээр үндэслээд 45-аас дээш насны эмэгтэйчүүдийг СА 125 тодорхойлох тандалтанд оруулж, энэ ИХМ-ын хэмжээ >30 IU/ml байгаа тохиолдолд өндгөвчийг хэт авиагаар шинжилж, эзлэхүүн нь >8,8 мл бол мэс ажиллабар хийж хавдар авах тандалт-эмчилгээний хувилбарыг санал болгосон байна (60, 61, 62).
Манайд судлагдсан байдал. Манай улсад СА-125-ыг судласан материалыг бид хэвлэлээс олсонгүй.
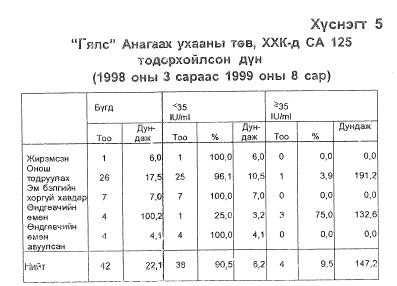
Гялс" Анагаах ухааны төв, ХХК-д 1998 оны 3 дугаар сараас СА 125-ыг Францийн bioMerieux компанийн mini-VIDAS хэмээх ФХТЭБУ-ын бүрэн автоматаар тодорхойлж байгаа бөгөөд 1999 оны 8 дугаар cap хүртлэх хугацаанд нийт 42 сорьцонд шинжилгээ хйиснээс энэ эсрэгтөрөгч 4(9,5%)-д нь >100 IU/ml хэмжээгээр тодорхойлогдсоны 3 нь эмнэлзүйн хувьд ӨӨ оноштой байсан хийгээд ӨӨ авхуулсаны дараах байдалтай 4 сорьцонд дунджаар 4,1 IU/ml тодорхойлогдсон (Хүснэгт 5) нь энэ ИХМ-ыг эмнэлзүйн практикт нэвтрүүлэх бололцоотой бөгөөд гүнзгийрүүлсэн судалгаа хийх шаардлагатайг харуулж байна.
СА-15-3
Тодорхойлолт. CENTOCOR компани СА 15-3 хэмээн нэрлэж анх үйлдвэрлэн хангаснаар энэ нэрийг авсан эсрэггөрөгч нь хөхний шүүрлийн эдээс ялгардаг 300-400 kDA молекул жинтэй гликопротейн (63) бөгөөд хүний хөхний булчирхайн тосон бөмбөлөгийн сарьсны эсрэг 115D8 моноклон (64) болон хөхний өмөн(ХӨ)-гийн эдийн эсрэг DF3 моноклон (65) сонгон таньдаг хоёр гол эпитоптой болно.
Эмнэлзүйн холбогдол. СА 15-3 нь төрөх насны жирэмсэн бус эмэгтэйчүүдийн ийлдсэнд 15-35 IU/ml тодорхойлогдож болох бөгөөд жирэмсэн үед 50 IU/ ml хүртэл ихэсч болно (2, 66, 67, 68). Энэ ИХМ-ын хэмжээ ХӨ-ийн 70-90%-д нь >30 IU/ml болж нэмэгдэх ба хавдрын болон үсэрхийлэлийн тархалтын зэрэглэлээс хэмжээ нь шууд хамааралтай тул ХӨ- ийн эмчилгээний үр дүнг хянахад голчлон ашигладаг.
Тарвалзүйн холбогдол. СА 15-3 тодорхойлох нь ХӨ-г эрт илрүүлэх нийтээр хүлээн зөвшөөрөгдсөн арга болох маммаграммын шинжилгээнээс давуу үзүулэлт байхгуй тул тарвалзүйн холбогдол багатай (3).
Манайд судлагдсан байдал. Манай улсад СА 15-3-ыг судласан материалыг бид хэвлэлээс олсонгүй.
Гялс" Анагаах ухааны төв, ХХК-д 1999 оны нэгдүгээр сараас СА 15-3-ыг Францийн bioMerieux компанийн mini-VIDAS хэмээх ФХТЭБУ-ын бүрэн автоматаар тодорхойлж байгаа бөгөөд 1999 оны 8 дугаар cap хүртлэх хугацаанд нийт 22 сорьцонд шинжилгээ хйихэд зөвхөн нэг (4,5%)-д нь СА 15-3 эсрэгтөрөгч >30 IU/ml хэмжээгээр тодорхойлогдсон байна. Үүний дотор ХӨ оноштой 6 өвчтөний сорьцноос зөвхөн нэг(16,7%)-д нь л СА-15-3 эсрэгтөрөгч 39,4 IU/ml хэмжээгээр тодорхойлогдсон нь энэ ИХМ-ыг оношлолын зориулалтаар бус, эмчилгзэний үр дүнг хянах зорилгоор ашиглах нь илүү үр дүнтэй болох тухай дээр дурьдсан судлаачдын дүгнэлттэй үндсэндээ дүйж байна.
Хүний хорионы гонадотропин (ХХГ)
Тодорхойлолт. ХХГ (hCG - human chorionic gonadotropin; Merck index 4534) нь эхсийн үндсэн гормон бөгөөд физиологийн ангиллаар өнчин тархины фолликул сэдээгч гормон (FSH: follicle stimulating hormone), шар биеийн гормон(LH: luteinising hormone)-ны хамт гонадотроп (бэлгийн булчирхайд нөлөөлөгч) гормоны, химийн ангилаар гликопротейд гормоны бүлэгт багтдаг, α болон β гэсэн 2 хэлхээнээс бүрдэл болдог 237 амин-хүчлийн үлдэгдлээс тогтсон, 30 орчим kDA молекул жинтэй уураг болно (69, 70). ХХГ-ы α хэлхээний нийлэгшлийг хариуцсан ген нь 18 дүгаар хромосом дээр, (3 хэлхээний нийлэгшлийг хариуцсан ген нь 19 дүгээр хромосом дээр тус тус байрладаг ажээ (71, 72).
Энэлзүйн холбогдол. ХХГ нь жирэмслэснийг илрүүлэх гол маркер бөгөөд ийлдсэндэх хэмжээ нь эрүүл эрэгтэйчүүдэд <3 mlU/ml, төрөх насны жирэмсэн бус эмэгтэйчүүдэд <5 mlU/ml, цэвэрших насны эмэгтэйчүүдэд <10 mlU/ml байдаг бол жирэмсний эхний долоо хоногоос ихэсч, 8-10 дахь долоо хоногт дээд цэгтээ (дунджаар 100 000 - 105 000 mlU/ml, дээд тал нь 220 000 mlU/ml) хүрч, цаашдаа аажмаар буурсаар жирэмсний 2 дахь триместрт дунджаар 31 000 mlU/ml, 3 дахь триместрт дунджаар 23 000 mlU/ml болдог байна (5). Жирэмсэн бус хүний ийлдэс, шээсэнд ХХГ ихсэх нь трофобласт эдийн гаралтай хавдар гэсэн онош тавих үндэслэл болох бөгөөд тиим хавдрын зэрэглэл, эмчилгээний үр дүнг хянахад энэ маркерийг мөн ашиглаж болно (2, 3, 15).
Тарвалзүйн холбогдол. ХХГ-ыг хавдрын тарвал зүйн зориулалтаар ашигласан хэвлэлийн материалыг бид олсонгүй.
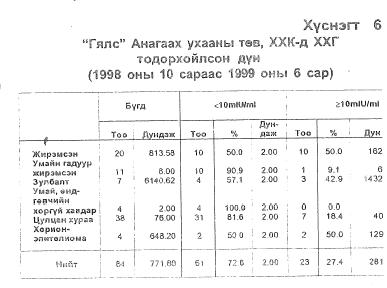
Гялс" Анагаах ухааны төв, ХХК-д 1998 оноос ХХГ-ыг Францийн bioMerieux компанийн mini-VIDAS хэмээх ФХТЭБУ--ын бүрэн автоматаар тодорхойлж байгаа бөгөөд 1999 оны 6 дугаар cap хүртлэх хугацаанд нийт 84 сорьцонд шинжилгээ хийснээс 23(27,4%)-д нь, үүний дотор трофобластын гаралтай хавдрын оноштой 42 өвчтөний 9(21,4%)-д нь XXГ >10mlU/ml хэмжээтэй тодорхойлогдсон байна (Хүснэгт 6).
ХХГ-ны хэвийн тархалтын зүй тогтолын Монголын онцлогийг судлан тогтоох, эх барих-эмэгтэйчүүдийн болон хавдар судлалын эмгэгийн оношлогоо, эмчилгээний үр дүнгийн хяналтанд ХХГ-ыг ашиглах бололцоог судлан тогтоох нь манай практикийн анагаах ухааны тулгамдсан асуудлын нэг болж байна.
Тодорхойлолт. Шүлтлэг фосфатаза (EC 3.1.3.) нь органик нэгдлээс фосфорын хүчлийн үлдэгдлийг салгадаг гидролазын бүлгийн фермент бөгөөд ЭШФ (placental alkaline phosphatase- PLAP) бол хүний шүлтлэг фосфатазын 4 изо-хэлбэрийн нэг, 120 kD молекул жинтэй, 532 аминхүчлийн үлдэгдлээс тогтсон димер уураг болно. (73, 74; NCBI-BLAST: Locus PPBN_HUMAN, Accession P 10696). Хүний ЭШФ-ын нийлэгшлийг хариуцсан ген нь 2 дугаар хромосом дээр байрладаг ажээ (75, 76).
Эмнэлзүйн холбогдол. ЭШФ нь хэвийн үед цусны ийлдсэнд тодорхойлогдохгүй, харин төмсөг, сэрээ булчирхайн эдэд иммуно-гисто-химийн аргаар ор төдий илрүүлж болдог бөгөөд семинома, ӨӨ, умайн хүзүүний өмөнгийн үед цусны ийлдсэнд илэрдэг (77, 78, 79) тул энэ ИХМ-ыг дээрхи байрлалын хавдрын оношийг баталгаажуулах, эмчилгээний үр дүнг хянахад ашигладаг (3, 15).
Тарвалзүйн холбогдол. ЭШФ-ыг хавдрын тарвалзүйн судалгаанд ашигласан материалыг бид хэвлэлээс олсонгүй.
Манайд судлагдсан байдал. Манай улсад ЭШФ-ыг судласан материалыг бид хэвлэлээс олсонгүй.
Мэдрэлийн эс өвөрмөц энолаза /МӨЭ/
Тодорхойлолт. Энолаза (буюу 2-фосфор-D- глицерат гидролаза; EC 4.2.1.) нь гликолизын замын фермент бөгөөд 3 изо-хэлбэртэйгэзс МӨЭ (nеиronе specific enolase- NSE) нь 434 амин хүчлийн үлдэгдлээс бүрддэг димер уураг юм. (NCBI-BLAST: Locus ENOG_HUMAN, Accession РР09104). Хүний МӨЭ-ын нийлэгшлийг хариуцсан ген нь 12 дугаар хромосом дээр байрладаг байна (80).
Эмнэлзүйн холбогдол.
Хэвийн үед энэ фермент зөвхөн мэдрэлийн эдэд л нийлэгждэг бөгөөд цусны ийлдсэн дэхь хэмжээ нь <12,5 ng/ml байдаг бол мэдрэлийн эдийн болон уушгины өмөн зэрэг хорт хавдрын үед идэвхи нь олон дахин ихэсдэг байна (81, 82, 83, 84). Тиймээс энэ ИХМ-ыг дээрхи байрлалын хавдрын оношийг баталгаажуулах, эмчилгээний үр дүнг хянахад ашигладаг (3, 15).
Тарвалзүйн холбогдол.
МӨЭ-ыг хавдрын тарвалзүйн судалгаанд ашигласан материалыг бид хэвлэлээс олсонгүй.
Манайд судлагдсан байдал. Манай улсад МӨЭ-ийг судласан материалыг бид хэвлэлээс олсонгүй.
44. Koprowski, Н., Steplewski, Z.Mitchell, К. et aI (1979): Colorectal carcinoma antigens detected by hybridoma anti¬bodies, Somatic Cell Genet 5(6): 957-71;
45. Brockhaus, M.Magnani, J.L.Blaszcyk, M et al. (:L9B1): Monoclonal antibodies directed against the human Leb blood group antigen, J.Boil Chem 256(24): 13223-5,
46. Magnani, J.L, Nilsson, B., Brockhaus, M. et aL (1982): A monoclonal-anlibod y-defined antigen associated with gastro-intestinal cancer is ganglioside containing sialylaied lacto-N-fucopentaose J.Boil Chem 257(23): 14365-9
47. Magnani, J.L,, SiepSewski, Z.Koprowski, H.Ginsburg, V. (1983): Identification of the gastrointestinal and pancreatic cancer-assosiated antigen detected by monoclonal antibody 19-9 in the sera of patients ac a mucin,Cancer Res 43(11): 5489-92;
48. Raux, H. Labbe, F., Fondaneche, M.C. et al. (1983): A study of gastrointestinal cancer-associated antigen (GICA) in human fetal organs, int. J. .Cancer, 32(3): 315-9:
49. HerIyn, M, Sears, H.F., Verril, H.( Koprowski, H. (1984): increased sensitivity in deleciing tumor-associsied antigens in sera of patients with colorectal carcinoma, J Immunol Methods, 75(1): 15-21;
50. Brockhaus, M., Wysocka, M., Magnani, J.L. et al. (1935): Normal salivary mucin contains the gastro-intestinaI cancer-associated antigen detected by monoclonal antibody 19-9 in the serum mucin of patients, Vox Sang., 48(1): 34-8;
51. Omtoft, T.F., Vestergaard, E.M., Holmes, E.H. et al. (1991): Influence of 1-3/4-L4-L-fucosyltransferase (FUT3) gene mutations on enzyme activity, erythrocyte phenoiyping and circulating tumor marlier syayl-Lewis a levels, J.Boil Chem 271: 32260-8;
52. Vertergaard, E.M., Hein, H.O., Meyer, H. et al. (1999):, Reference values and biological variation for tumor marker CA 19-9. in serum for different Lewis and secretor genotypes and evaluation of secretor and Lewis genotyping in a Caucasian population, Clin. Chem.: 45(1): 54-61;
53. Tizzani, A., Caseita, G., Cicigoil, A. et al. (1987):
Tumor markers (CEA, TPA and CA 19-9) in urine of bladder cancer patients, Int. J. Biol. Markers, 2: 121-4;
54. Casetta, G., Piana, P., Cavallini, A. et al. (1993): Urinary levels of tumor associated antigens (CA 19-9, TPA and CEA) in patients with neoplastic and non-neoplastic urothelial abnormalities, Br. J. Urol., 72: 60-4;
55. Verstergaard, E.M., Wolf, H., Orntoft, T. (1998): In¬creased concentrations of genotype-interpreted CA 19-9 in urine of bladder cancer patients mark diffuse atypia of the urothelium, Clin. Chem.: 44(2): 197-204;
56. Bast, R.C., Feeney, fvl, Lazarus, H. et al. (1981): Reactivity of a monoclonal antibody with human ovarian carci¬noma, J.Clin Invest , 68(5): 1331-7;
57. Kenemans, P.,Yedema, C.A.,Bon, G.G., Mensdorff-
Pouilly, S. (1993): CA 125 in gynecological pathology - a re-
view, Eur, J.Obstet Gynecol, Reprod, Biol 49(1-2): 115-24;
58. van Ingen, H.E., Chan, D.W., Hubl, W. et al. (1.998): Analytical and clinical evaluation of an electrochemiluminescence immunoassay for the determination of CA 125, Clin. Chem„ 44(12): 2530-6;
59. van Dalen, A. (1993): Quality control and standard¬ization of tumor marker tests, Tumor Diagn. Ther., 14: 131-5;
60. Jacobs, I., Stabile, I., Bridges, J. et al. (1988): Multimodal approach to screening for ovarian cancer, Lancet, I: 268-71;
61. Jacobs, I., Davies, A.P., Bridges, J. et al. (1993): Prevalence screening for ovarian cancer in postmenopausal women by CA 125 measurement and ultrasonography, BMJ, 306: 1030-4;
62. Jacobs, I., Skates, 8., Davies, A.P., et al. (199.6): Risk of diagnosis of ovarian cancer after raised serum CA 125 concentration: a prospective cohort study, BMJ, 313: 1355-8;
63. Gendler, S.J., Spicer, A.P., Lalani, E.N. et al. (1991): Structure and biology of a carcinoma-associated mucin, Muc-1, Am, Rev, Respir, Dis 144: S42-7;
64. Milkins, J., Bwjs, F., Hilgers, J. et al. (1984): Mono¬clonal antibodies against human milk fat globule detecting dif¬ferentiating antigens of the mammary gland and its tumours, J.Cancer , 34: 197-207;
65. Kufe, D., IngNrami, G., Abe, M. et al. (1934): Differ¬ential reactivity of a novel monoclonal antibody (DF3) with hu¬man malignant versus beningn breast tumours, Hybridom.a, 3: 223-32;
66. Hayes, D.F., Zurawski, V.R., Kufe, D.W. (19.36): Comparison of circulating CA 15-3 and CEA levels in patients with breast cancer, J. Clin. Oncol., 4(10): 1542-50;
67. Safi, F., Kohter, I., Rottinger, E. et al. (1939): Com¬parison of CA 15-3 and CEA in diagnosis and monitoring of braest cancer, int, J.Biol Markers , 4(4): 207-14;
68. Cheli, CD., Morris, D.L., Kish, L. et al. (1993): Multicenter evaluation of the Bayer immuno 1 ™ CA 15-3 as¬say, Clin Chem , 44(4) 765-72;
69. Уайт, A., Хендлер, Ф., Смит, Э., Хилл, P., Леман, И. (1931): Соновы биохимии, В трёх томах, перевод с английского, т.З, с. 1683-90;
70. Lapthom, A.J., Harris, D.C., Littlejohn, A. et al. (1994): Crystal structure of human chorionic gonadotropin, Nature, 369(6480): 455-61;
71. Hardin, J.W., Riser, M.E., Trent, J.M., Kohler, P.O. (1933): The chorionic gonadotropin alpha-subunit gene is on human chromosome 18 in JEG cells, Proc. Natl. Acad. Sci. USA, 80(20): 6282-5;
72. Julier, C, Weil, D„ Couillin, P. et al. (1934): The beta chorionic gonadotropin - beta luteinizing gene cluster maps to chromosome 19, Hum. Genet, 67(2): 174-7;
73. Holmgren, PA, Stigbrand, T. (1976): Purification and partial characterization of two genetic variants of placental al¬kaline phosphatase, Biochem Genet, 14(9-10):777-89;
74. Holmgren, P.A., Stigbrand, T., Beckman, G. (19Z7): Purification and partial characterization of the I variant of pla¬cental alkaline phosphatase, Biochem Genet, 15(5-6): 521¬30;
75. Kam, W. Clauser, E., Kim, Y.S. et al., (№35): Clon¬ing, sequesncing, and chromosomal localization of human term placental alkaline phosphatase cDNA, Proc. Natl. Acad. Sci., 82(24): 8715-9;
76. Martin, D., Tucker, D.F., Gorman, P. et al., (1931): The human placental alkaline phosphatase gene and related sequences map to chromosome 2 band q37, Ann. Hum. Genet., 51 (Pt 2): 145-52;
77. Kellen, J.A., Bush, R.S., Malkin, A. (1916): Placenta¬like, alkaline phosphatase in gynecological cancers, Cancer Res., 36(1): 269-71;
78. Malkin, A., Kellen, J.A., Lickrish, G.M., Bush, R.S. (191&): CEA and other tumor markers in ovarian and cervical cancer, Caocer, 42(3 Suppi.): 1452-6;
79. Lange, P H., Millan, J.L, Stigbrand, T. et al. (1982): Placental alkaline phosphatase as a tumor marker for semi¬noma, Cancer Res,, 42(8): 3244-7;
80. Ansari-Lari, MA., Muzny, D.M., Lu, J. et al. (1993): A gene-rich cluster between the CD4 and triosephosphate isomerase genes at human chromosome 12p13, Genoma Res., 6(4): 314-26;
81. Tapia, F.J., Polak, J.M., Barbosa, A.J. et al. (1*931): Neuron-specific enolase is produced by neuroendocrine tumours,Lancet , 1(8224): 808-11;
82. Carney, D.N., Marangos, P.J., Ihde, D.C. et al. (1932): Serum neuron-specific enolase: a marker for disease extent and response to therapy of small-cell lung cancer, Lancet, 1(8272): 583-5;
83. Ariyoshi, Y., Kato, K., Ishiguro, Y. et al. (1983): Evalu¬ation of serum neuron-specific enolase as a tumor marker for carcinoma of the lung, Gann, 74(2): 219-25;
84. Massaron, S., Seregni, E., Luksch, R. et al. (1993): Neuron-specific enolase evaluation in patients with neuroblas¬toma, Tumour BioL, 19(4): 261-3;