АШУҮИС, Эмзүй-БиоАС, Эсийн биологи, биохимийн тэнхим
Background
Hydroquinone (1,4 di-hydroxy benzene) is an aromatic organic compound with diverse biological functions that are commonly used as pigment or cosmetic additives. Its chemical structure has two hydroxyl groups bonded to a benzene ring in a para position. In the nature hydroquinone have a primary reagent in the defensive glands of bombardier beetles, along with hydrogen peroxide, which collects in a reservoir [1]. Hydroquinone glycoside form is 4-hydroxyphenyl-α-D-glucopyranoside (α- Arbutin). Arbutin is a potent inhibitor of melanin synthesis and has been reported to possess inhibitory activity on lipid peroxidation and is used in the cosmetic industry for its antibacterial and skin lightening effects [9]. It is faster and more effictive another commonly used skin lightener, even at use very low concentrations.
Material and Methods
The in vitro glycosylation reaction was carried out as described in materials and methods. DNA was extracted than E.coli BL 21 and E.coli JM 109 hosts were used for expression of proteins. The purified protein was then analyzed by 12% SDS-PAGE than used for enzymatic recycle system. Hydroquinone reaction mixture was incubated at 37өC for 8 and 24 hour than quenched by heating in boiling water for 10 min. The reactions products was first analyzed by TLC followed by HPLC analysis.
Results
This work substrate hydroquinone for the enhancement of enzymatic recycling system glycosylation. TLC and HPLC analyses of the products were carried out to the recycled system worked and glycosylation product.
Conclusion
In this study, hydroxyl groups of the para position of hydroquinone involved for glycosylation to compare with standards were analysed by TLC and HPLC. When the compared 8 hour reactions obtained the apparent glycosylation and stability of the recycling system.
Key word: Arbutin, Glycosylation, Glycosyltransferse, Hydroquinone, HPLC, TLC.
Pp. 14-17, Figures 4, References 10
Удиртгал
Гидрохинон нь биологийн идэвхитэй, үнэрт органик нэгдэл бөгөөд ихэвчлэн гоо сайханы нэмэлт эсвэл пигмент болгон ашиглаж байна. Химийн бүтцийн хувьд бензолийн цагирагтай пара байрлалтай хоёр гидроксил бүлэг агуулсан. Байгаль дээр Brachinus species цохны хамгаалах булчирхайнд устөрөгчийн хэт исэлтэй хамт нөөцлөгдөж байдаг.
Арбутин бол гидрохиноны гликозилжсэн хэлбэр бөгөөд меланины синтезийг хүчтэй саатуулагч, липидийн хэт исэлдэлтийг идэвхитэй саатуулдаг байна. Гоо сайхны бүтээгдэхүүн үйлдвэрлэгчид арбутиныг арьс цайруулах бага концентрацитай уусмал байдлаар буюу нянгийн эсрэг бүтээгдэхүүний зорилгоор үйлдвэрлэж байна.
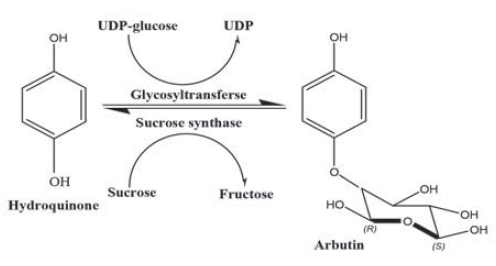
Figure 1. Schematic reaction pathway of recycling system.
Энэхүү судалгаанд гидрохинонын гликозилжуулахад ресайкл системийг хэрэглэсэн. (Зураг 1).
Зорилго
Глюкозилтрансфераза (YjiC) болон сахарозсинтазаг (AtSUS1) ферментийг ашиглан гликозилжсэн гидрохинон (арбутин) гаргаж авах, ресайкл системийн гликозилжилтэд хугацааны хамаарлыг холбох судалгааны зорилго дэвшүүллээ.
Материал, аргазүй
Рекомбинант глюкозилтрансфераза YjiC-ийн генийг Bacillus licheniformis DSM 13 омгоос ялган авч, Arabidopsis thaliana–аас сахарозсинтазагийн генийг ялган авч E.coli-д экспресслэсэн. E.coliийн омгуудыг LB тэжээлт орчинд өсгөвөрлөн, ультра соникатороор задлан центрифугдэж, уусамтгай уургийн фракцаас ферментийг өндөр даралтат шингэний хроматографийн аргаар ялган, цэвэршүүлсэн. Ялгасан уургийн фракцыг 12% SDS-PAGE-д шалгасан. Өтгөрүүлсэн дээжид сахар 100 мМ, гидрохинон 100 мМ, YjiC 5 μЛ, AtSUS1 15 μЛ болон УДФ-гликозийг 2 мМ, 4мМ болон 8 мМ-ийн концентрацад тус тус 8 цаг болон 24 цаг бэлтгэсэн. Нимгэн үеийн хроматографийн (TLC) аргаар болон шингэний хроматографийн (HPLC) аргаар гидрохиноны гликозилжсэн урвалын бүтээгдэхүүнийг шалгасан.
Үр дүн, хэлцэмж
Рекомбинант глюкозилтрансфераза YjiC уургийн фракцийг SDS-PAGE-д шалгахад тод зурвас ялгаран харагдаж байгаа нь экспресс амжилттай болж концентраци харьцангуй өндөр байгааг гэрчилж байна. Мөн сахарозсинтаза AtSUS1 уургийн фракц SDS-PAGE-д шалгахад бүдэг зурвас ялгаран харагдаж байгаа нь концентраци харьцангуй бага байгааг харуулж байна. Их концентрацитай глюкозилтрансфераза YjiC уураг нь бага концентрацитай сахарозсинтазагийн AtSUS1 уургийн идэвхийг дарангуйлснаар ресайкл систем явагдахгүй эсвэл бүтээгдэхүүний гарц бага байж болох юм. Иймээс AtSUS1-ийн концентрацийг нэмэгдүүлэх зорилгоор өтгөрүүлэгч (centricon) –ийг хэрэглэсэн.
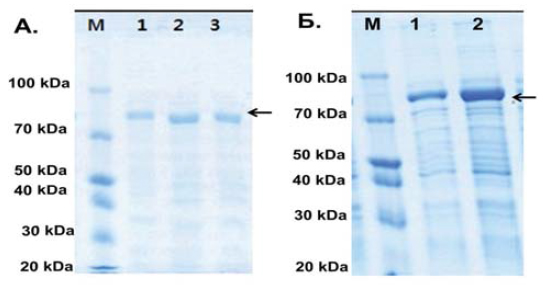
Figure 2. SDS – PAGE of purified AtSUS1 protein. A. Before used centricon M, Protein marker;(88kDa), Lane 1, Purified AtSUS1soluble protein eluted by 10 mM imidazole; Lane 2, Purified AtSUS1 soluble protein eluted by 100 mM imidazole, Lane, 3 Purified AtSUS1soluble protein eluted by 200 mM imidazole. Б. After used centricon M, Protein marker;(88kDa), Lane 1, Purified AtSUS1soluble protein eluted by 10 mM imidazole; Lane 2, Purified AtSUS1 soluble protein eluted by 100 mM imidazole.
Үр дүнгээс харахад 100мМ imidazole-д цэвэршүүлсэн AtSUS1-ийн концентраци нэмэгдэж харьцангуй өндөр болсныг гэрчилж байна.
Молекул массын хувьд 88 kDa байгаа нь тохирч байна.
Нимгэн үет хроматографийн үр дүн
Стандарт сахароз, УДФ-гликоз, гидрохинон болон УДФ-гликозгүй хяналтийн өтгөрүүлсэн дээжээ харьцуулан нимгэн үеийн хроматографийн аргаар шалгахад шинэ цэг үүссэн нь гликозилжсэн бүтээгдэхүүн байгааг гэрчилж байна.
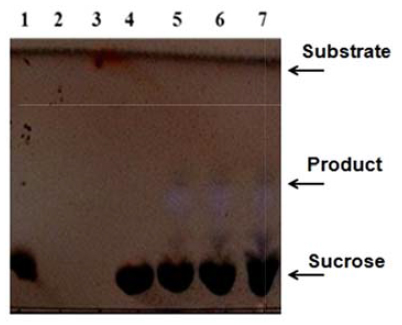
Figure 3. TLC analysis of in vitro glycosylation of hydroquinone. 1.Sucrose 100mM, 2. UDP-glucose 8 mM, 3. Hydroquinone 100mM, 4. Control without UDPglucose, 5. Rxn-with 2mM UDP-glucose, 6. Rxn-with 4mM UDP-glucose, 7.Rxn-with 8mM UDP-glucose.
Нимгэн үеийн хроматографийн уусгагчуудаар этил ацетат; цууны хүчил; нэрмэл ус (3: 1: 1) тус тус ашигласан (Зураг 3).
Өндөр даралтад шингэний хроматографийн үр дүн
Ресайкл системийн гликозжсон 8 цаг болон 24 цагийн өтгөрүүлсэн дээжээ 290 нм-ийн хэт яагаан туяаны шингээлтийг ашиглаж өндөр даралтад шингэний хроматографийн (HPLC) аргаар ялгасан.
Босоо тэнхлэгийн дагуу гликозжилтийн хэмжээ, хэвтээ тэнхлэгийн дагуу гликозжсэн бүтээгдэхүүн илэрсэн минутийг харуулж байна.
Стандарт гидрохинон 4.5 минутанд хоёр шинэ фракц 3.7 минут болон 3.1 минутанд тус ялгарсан нь гликозжсон бүтээгдэхүүн байгааг илтгэж байна (Зураг 4).
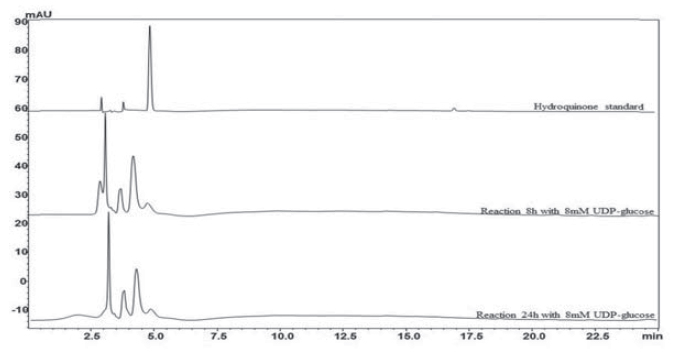
Figure 4. HPLC analysis profile comporation of standard and reactions
Дүгнэлт
Дээрх судалгааны дүнгээс үзэхэд гидрохиноны пара байрлал дахь гидроксилийн бүлгүүд НҮХ/ ӨДШХГ аргаар тодорхойлоход гликозилжсэн стандартай харьцуулсан дүнгээр батлагдаж байна.
8 цаг болон 24 цагийн хугацаанд өтгөрүүлсэн дээжээ харьцуулхад 24 цагт гидрохинон илүү тогтворжиж гликозилжсэн байгаа нь ресайкл системд удаан хугацааны гликозжилт илүү үр дүнтэй байгаа нь харагдаж байна.
2. Baud, Sйbastien., et al. Structure and expression profile of the sucrose synthase multigene family in Arabidopsis. “J. Exper. Bot”, 55, 2004, pp 397-409.
3. Castellano, G., Tena, J., & Torrens, F. (2012). Classification of phenolic compounds by chemical structural indicators and its relation to antioxidant properties of Posidonia oceanica (L.) delile. Environment, 2, 6.
4. Jerkovic, V., Nguyen, F., Nizet, S., & Collin, S. (2007). “Combinatorial synthesis, reversedphase and normal-phase high-performance liquid chromatography elution data and liquid chromatography/positive atmospheric pressure chemical ionization tandem mass spectra of methoxylated and glycosylated resveratrol analogues. Rapid communications in mass spectrometry, 21, 2456-2466.
5. Jimbow, K., Obata, H., Pathak, M. A., & Fitzpatrick, T. B. (1974). Mechanism of depigmentation by hydroquinone. Journal of Investigative Dermatology, 62, 436-449.
6. Masada, Sayaka., et al. An efficient chemoenzymatic production of small molecule glucosides with in situ UDP-glucose recycling. ”FEBS Lett”, 581, 2007, pp 2562-2566.
7. Matsuba, Y., Okuda, Y., Abe, Y., Kitamura, Y., Terasaka, K., Mizukami, H., Ozeki, Y. (2008). Enzymatic preparation of 1-O-hydroxycinnamoyl- β-D-glucoses and their application to the study of 1-O-hydroxycinnamoyl-β-D-glucose-dependent acyltransferase in anthocyanin-producing cultured cells of Daucus carota and Glehnia littoralis. Plant biotechnology, 25, 369-375.
8. Ozaki, S. I., Imai, H., Iwakiri, T., Sato, T., Shimoda, K., Nakayama, T., & Hamada, H. (2012). Regioselective glucosidation of trans resveratrol in Escherichia coli expressing glucosyltransferase from Phytolacca americana. Biotechnology letters, 34, 475-481.
9. Seo, D. H., Jung, J. H., Ha, S. J., Cho, H. K., Jung, D. H., Kim, T. J., ... & Park, C. S. (2012). Highyield enzymatic bioconversion of hydroquinone to α-arbutin, a powerful skin lightening agent, by amylosucrase. Applied microbiology and biotechnology, 94 , 1189-1197.
10. Terasaka, Kazuyoshi., et al. In situ UDP-glucose regeneration unravels diverse functions of plant secondary product glycosyltransferases. “FEBS Lett”, 586, 2012 pp 4344-4350.




