1 ЭМШУИС, ЭЗС- магистрант
2Монос групп
3ЭМШУИС, Эм зүйн сургууль
Introduction: Amlodipine is one of the products included in Mongolian Essential Medicine list. Local drug manufacturers don’t produce this product and our country imports this product from several countries. Drug research institute has developed the technology to produce Amlodipine 10 mg tablet on the scientific basis and quality study has to be performed.
Goal: The aim of this study was to define suitable conditions of quantitative determination and in vitro bioequivalence study of Amlodipine 10 mg tablet developed by Drug research institute.
Materials and Methods: Assay method was developed using British and Russian pharmacopeia [5,7] and international journals [8,9]. High performance liquid chromatography (HPLC) separation was performed using Shimadzu HPLC with UV detection which is analytical column Оctadecylsilane (150x4.6 mm, particle
size 5 μm). Separation took place at 40oC, flow rate of mobile phase (buffer-acetonitrile-methanol, 50:15:35) was 1.0 ml/min. Normodipine and Amlodenk used as standard medicine.
Results: In the framework of this study HPLC and spectrophotometer method to determine amlodipine content was developed. The amlodipine content was determined by both methods as 0.0108 g and 0.0109 g respectively. Amlodipine dissolution was 110%, Normodipine dissolution was 110%, Amlodenk 109%.
Conclusions: Assay method of Amlodipine 10 mg tablet was developed. Quality criteria of the tablet were determined and manufacturer’s pharmacopiea’s monograph for Amlodipine 10 mg tablet was developed. Amlodipine was bioequivalence with standard medicines.
Удиртгал:
Зүрх судасны тогтолцооны өвчлөл жилээс жилд нэмэгдсээр байгаа ба Монгол улсын хүн амын нас баралтын тэргүүлэх шалтгаанынэгдүгээрт (10000 хүн амд 22.6), хүн амын өвчлөлийн тэргүүлэх шалтгааны дөрөвт уг өвчин орж байна [1]. Зүрх судасны тогтолцооны өвчлөлд цусны даралт ихсэх өвчин хамгийн түгээмэл тохиолддог байна.
Цусны даралт ихсэх өвчин 2011 оны байдлаар Монгол улсын нийт өвчлөлийн 3,8 %-ийг эзэлж,10000 хүн амд 311,8 тохиолдсон байна [2]. Цусны даралт бууруулах үйлдэлтэй Амлодипин 5, 10 мг шахмал эм хэдийгээр Монгол улсын зайлшгүй шаардлагатай эмийн жагсаалтанд орсон [3], манай оронд өргөн хэрэглэдэг эмийн бэлдмэлийн нэг боловч уг бэлдмэлийг эх орны эмийн үйлдвэрүүд үйлдвэрлэдэггүй, өөрийн орны хэрэгцээг импортын бүтээгдэхүүнээр хангаж байна. Монгол улс Амлодипин 5, 10 мг шахмал эмийг
Германы Денк фарм, Унгарын Ге деон Рихтер, Энэтхэгийн Aurobindo Pharma, Cipla Ltd, Америкийн Novartis, Словенийн KRKA болон бусад орны эмийн үйлдвэрүүдээс импортлон хэрэглэж байгаа ба 2011 оны байдлаар Монгол улсын эмийн бүртгэлд нийт 21 нэр төрлийн амлодипин бүртгэгдсэн байна [4]. Монгол улс эмчилгээний практикт өргөн хэрэглэдэг, өндөр идэвхитэй, чанартай эмийн бэлдмэлүүдийг эх орондоо үйлдвэрлэн өөрийн эх орны эмийн бэлдмэлийн нэр төрлийг нэмэгдүүлэх зайлшгүй шаардлагатай байна. Эм судлалын хүрээлэнд Амлодипин 10 мг эмийг үйлдвэрлэх технологийг боловруулсан ба уг технологийг ашиглан үйлдвэрлэсэн эмийн чанарын шалгуур үзүүлэлтийг тогтоон, тухайн бэлдмэлийн фармакопейн өгүүллийг боловсруулах шаардлагатай байна.
Зорилго, зорилт: Уг судалгааны ажлын зорилго нь амлодипин 10 мг шахмал эмийг стандартчилах гол үзүүлэлт болох тооны тодорхойлолтыг хийж, стандарт эмийн хэлбэрүүдтэй харьцуулахад оршино.
Үүний тулд дараах зорилтуудыг тавив.
1. А млодипины тооны агууламжийг тогтоох аргачлалыг боловсруулах
2. Шахмал эмэнд тавигдах гол чанарын шалгуур үзүүлэлтүүдийг тодорхойлж, үйлдвэрлэгчийн фармакопейн өгүүллийн төсөл боловсруулах
3. Т уршилтын Амлопидин шахмал эмийн уусалтыг дэлхийн шилдэг эмийн үйлдвэрийн бүтээгдэхүүний уусалттай харьцуулах
Судалгааны материал, арга зүй: Эм судлалын хүрээлэнд туршилт судалгааны дүнд үйлдвэрлэсэн Амлодипин 10 мг шахмал эмийг судалгаанд ашиглав. Амлодипин 10 мг шахмал эмэнд агуулагдах амлодипины тоон агууламжийг тодорхойлох аргачлалыг SHIMADZU фирмийн ӨИШХ багажийг ашиглан Их Британи болон Оросын фармакопейн Амлопидины бесилалтын өгүүлэлд [2,3] үндэслэн С18 (Оctadecylsilane жижиг хэсгийн хэмжээ 5 μкм, колонкийн урт 150 мм, диаметр 4.6 мм) колонк, баганын температур 40оС, хэт ягаан туяаны детектор 237 нм, Фосфатын буфер-аце тонитрил-метанол (50:15:35) хөдөлгөөнт фазын системд 1,0 мл/мин урсах хурдтайгаар 10 мин гүйлгэж тодорхойлох аргачлалыг боловсруулж, үйлчлэгч бодисын тооны агууламжийг тогтоов. Амлодипины агууламжийг тодорхойлох спектрофотометрын аргачлалыг олон улсын сэтгүүлд нийтлүүлсэн өгүүллийг [6,7] ашиглан хэт ягаан туяаны детектор 237 нм, 360 нм долгионы уртад этанол, ус, аце тонитрил-усны холимогийг уусгагчаар авч, SHIMADZU фирмийн UV mini 1240, UV-VIS спектрофотометр багажинд тодорхойлж боловсруулав. Стандарт бодисоор Sigma-Aldrich компанийн Амлодипины бесилатыг ашиглав. Стандарт эмийн хэлбэрээр Ге рманы Денк фарм “Амло-денк”, Унгарын Ге деон Рихтер “Нормодипин” эмүүдийг ашиглав. Задралт, уусалт зэрэг үзүүлэлтүүдийг SY-6D tablet tester багажаар тодорхойлов.
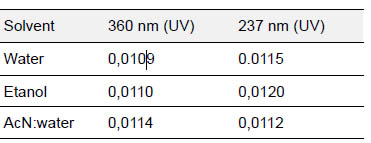
Судалгааны үр дүн: Амлодипин 10 мг шахмалд агуулагдах амлодипины агууламжийг спектрофотометрийн аргаар этанол, ус, аце тонитрил-усны холимогийг уусгагч болгон, гэрэл шингээлтийг 360 нм, 237 нм-ийн долгионы уртад хэмжиж тодорхойлсон үр дүнг 1-р хүснэгтэд үзүүллээ.
Table.1. The result of spectrophotometer method to determine amlodipine content.
Амлодипин 10 мг шахмалд агуулагдах амлодипины агууламжийг ӨИШХ-ийн аргаар тодорхойлох аргачлал болон спектрофотометрийн аргаар тодорхойлох аргачлалыг боловсруулсан ба амлодипины агууламжийг тодорхойлох хроматографийн хамгийн тохиромжтой нөхцөл болон спектрофотометрийн нөхцөлийг тогтоосныг
2-р хүснэгтэд үзүүллээ.
.jpg)
Шахмалд агуулагдах амлодипин бесилатын хэмжээ спектрофотометрээр тодорхойлоход 0,0109 г, ӨИШХ –иар тодорхойлоход 0,0108 г байв. Уусалт, задралт, тоон агууламж зэрэг үзүүлэлтийг стандарт эмүүдтэй харьцуулсан үр дүнг 3-р хүснэгтэд үзүүллээ.
Table 3. The result of comparative study of Amlodipine 10 mg.
.jpg)
Өөрсдийн туршилтаар үйлдвэрлэсэн Амлодипин 10мг шахмал эмийг дэлхийн шилдэг эмийн үйлдвэрүүд болох Ге рманы Денк фарм эмийн үйлдвэрийн “Амло-денк”, Унгарын Ге деон Рихтер фирмийн “Нормодипин” зэрэг эмийн бүтээгдэхүүнтэй харьцуулан судлав. Судалгааны үр дүнгээс харахад туршилтаар үйлдвэрлэсэн Амлодипин10мг шахмал эм нь Нормодипин 10 мг, Амлоденк 10мг бүтээгдэхүүнтэй биоэквивалент байлаа.Хэлцэмж: Амлодипины шахмал эм Монгол улсын зайлшгүй шаардлагатай эмийн жагсаалтанд орсон, манай орны эмийн эмчилгээний практикт өргөн хэрэглэгддэг эмийн бэлдмэлийн нэг боловч уг бэлдмэлийг эх орны эмийн үйлдвэрүүд үйлдвэрлэдэггүй, өөрийн орны хэрэгцээг импортын бүтээгдэхүүнээр хангаж байна. Энэхүү судалгаагаар Эм судлалын хүрээлэнд технологийг боловсруулсан Амлодипин 5, 10 мг шахмал эмэнд агуулагдах үйлчлэгч бодисын тоо хэмжээг тогтоох аргачлалыг боловсруулав.Ерөнхий нэршлийн эмийн чанар, аюулгүй байдлыг
сайжруулахад биоэквивалент чанарын судалгаа зайлшгүй шаардлагатай байдаг. Америкийн Эм, Хүнсний Удирдах газраас зөвлөмж болгосоны дагуу ерөнхий нэршлийн эм брэнд эмтэйгээ (80-120%) биоэквивалент бол үйлдвэрлэж болохыг заасан байдаг [7]. Эм судлалын хүрээлэнд боловсруулсан технологийн дагуу туршилтаар үйлдвэрлэсэн Амлодипин 10 мг шахмал эм “Амло-денк”,“Нормодипин” шахмал эмүүдтэй биоэквивалент байлаа.Энэхүү судалгааны дүнд Амлодипин 10 мг шахмал
эмийн үйлдвэрлэгчийн фармакопейн өгүүллийн төслийг боловсруулав.
Дүгнэлт
1. А млодипины тооны агууламжийг ӨИШХ болон спектрофотометрийн аргаар
2. тодорхойлох тохиромжтой нөхцөлийг тогтоов.
3. Шахмал эмэнд тавигдах гол чанарын шалгуур үзүүлэлтүүдийг тодорхойлж, үйлдвэрлэгчийн фармакопейн өгүүллийн төслийг боловсруулав.
4. А млодипин 10 мг шахмал эмийн үйлчлэгч бодисын агууламж, уусалт, задралт зэрэг үзүүлэлт стандарт эмийн бүтээгдэхүүнтэй биоэквивалент байна.
1. Эрүүл мэндийн статистик үзүүлэлтүүд, 2011 он,60 хуудас
2. Эрүүл мэндийн статистик үзүүлэлтүүд, 2011 он,57 хуудас 12 Монголын эм зҮй, эм судлал сэтгүүл
3. Монгол улсын зайлшгүй шаардлагатай эмийн 6-р жагсаалт, 2009
4. Монгол улсын эмийн бүртгэлийн жагсаалт, 2011 он, http://124.158.109.64:8080/licemed/ publicMedProduct,$Form.sdirect
5. Pournima Patil and etc, Spectrophotometeric method for simultaneous determination of amlodipine besylate and olmesartan medoxomil from tablet dosage form, Journal of Current Pharmaceutical Research, Vol 3, Issue 2, 2011
6. Sayed M.Derayea and etc, Spectrophotometeric determination of amlodipine besylate and nicardipine in pharmaceutical formulations, Jour of Appl. Pharma. Sc. 02(06) 2012, p.84-89.
7. USP30-NF25, general guidance; Food and Drug Administration Center for Drug Evaluation and Research, Guidance for Industry, 2000




